その「午後の眠気」、本当にただの疲れですか?
昼食後、デスクで襲ってくる強烈な眠気。集中力が途切れ、思考がまとまらない。多くのビジネスパーソンが経験するこの現象を、私たちは「食べ過ぎ」や「睡眠不足」のせいだと片付けてしまいがちです。
しかし、もしそのパフォーマンス低下が、日々の食事によって引き起こされる「血糖値スパイク」という、目に見えない生理的な乱高下が原因だとしたらどうでしょう。これは単なる体調の問題ではなく、あなたの知的生産性を静かに蝕む「機会損失」と言えるかもしれません。
こんにちは。医師・医学博士であり、AIやデータサイエンス、行動経済学の視点からヘルスケアを探求している髙﨑洋介です。
本記事では、多忙な日々を最高のコンディションで乗り切りたいと願うすべての方々へ、科学的根拠(エビデンス)とデータに基づき、「血糖値スパイク」の正体と、その手綱を握るための具体的な戦略を解説します。これは、自らの健康のCEOとして、最高のパフォーマンスを維持するための「知的武装」の書です。食事がもたらす影響をシステムとして理解し、日々の選択を最適化していきましょう。

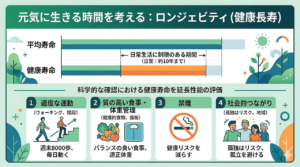
血糖値スパイクとは何か?見過ごされている「パフォーマンスの乱高下」
まず、「血糖値スパイク」とは何かを正確に理解することから始めましょう。これは医学的には「食後高血糖」と呼ばれ、食事、特に糖質を摂取した後に血糖値が急激に上昇し、その後、急降下する現象を指します。米国糖尿病学会(ADA)も、食後の血糖管理の重要性を指摘しています (American Diabetes Association, 2023)。
この血糖値のジェットコースターは、私たちの心身に二段階で影響を及ぼす可能性があります。
血糖値スパイクの概念図
1. 急上昇とその後の急降下が引き起こす「短期的な不調」
食事により血糖値が急上昇すると、私たちの身体は膵臓からインスリンというホルモンを大量に分泌して、血糖値を正常範囲に戻そうとします。しかし、このインスリンが過剰に分泌されると、今度は血糖値が必要以上に下がり、「反応性低血糖」に近い状態に陥ることがあります。
この状態が、食後の眠気、倦怠感、集中力の低下といったパフォーマンス低下の要因の一つと考えられています (Service, F. J. et al., 1983)。重要な会議や創造的な作業の前に、無意識に自らのパフォーマンスを低下させる選択をしてしまっている可能性があるのです。
2. 繰り返されるスパイクがもたらす「長期的な健康リスク」
さらに懸念されるのは、このスパイクが繰り返されることによる長期的な影響です。血糖値の急上昇は血管の内壁にダメージを与え、動脈硬化を促進する一因となることが指摘されています (Ceriello, A., 2005)。
また、過剰な糖は体内のタンパク質と結びつき、細胞を変性させる「糖化」という反応を引き起こします。この糖化は、加齢に伴う様々な変化に関与する可能性が報告されています (Brownlee, M., 2001)。
そして何より、インスリンを分泌する膵臓に常に過剰な負担をかけ続ける食生活は、将来的に2型糖尿病を発症するリスク因子の一つと考えられています (Ceriello, A., 2005)。これはまさに、気づかぬうちに積み重なる「健康負債」と言えるでしょう。
なぜ起こるのか?血糖値スパイクのメカニズムと「GI値」という羅針盤
では、なぜ血糖値スパイクが起こりやすい食事とそうでない食事があるのでしょうか。その鍵を握るのが、食事の内容、特に「糖質の質」です。
ここで重要な指標となるのが「GI値(グリセミック・インデックス)」です。これは、食品を摂取した後の血糖値の上昇度合いを示す指標であり、ブドウ糖を100とした場合の相対値で表されます。
- 高GI食品(GI値70以上): 白米、食パン、うどん、じゃがいも、菓子類など。消化・吸収が速く、血糖値を急激に上昇させやすい特徴があります。
- 低GI食品(GI値55以下): 玄米、全粒粉パン、オートミール、豆類、葉物野菜など。消化・吸収が穏やかで、血糖値の上昇も緩やかです。
このGI値の概念は、トロント大学のジェンキンス博士らによって1981年に医学雑誌『The American Journal of Clinical Nutrition』で提唱されて以来、栄養学の基本的な考え方となっています (Jenkins, D. J. et al., 1981)。
パフォーマンスを最大化する食事戦略:血糖値スパイクを抑制する5つの科学的アプローチ
血糖値の動態、すなわち血糖カーブを理解した今、次はいよいよ具体的な介入戦略について考察します。日々の知的・身体的パフォーマンスを安定させ、長期的なウェルビーイングという「健康資本」を築くための、科学的エビデンスに基づいた5つのアプローチをご紹介します。
本稿では、数多ある戦略の中から特に重要かつ実践的なものをダイジェストとして解説します。それぞれの詳細なメカニズムや応用については、今後の記事でさらに深掘りしていく予定です。
アプローチ1:食べる順番の最適化 — 「食物繊維・タンパク質・脂質」を先に
最も手軽かつ効果的な戦略の一つが、食事の中での「食べる順番」を最適化することです。一般に「ベジタブル・ファースト」として知られていますが、本質は「食物繊維・タンパク質・脂質を、炭水化物(糖質)より先に摂取する」ことにあります。
この戦略の背景には、2つの主要なメカニズムが存在します。
- 物理的な「壁」効果: 先に野菜などに含まれる豊富な食物繊維を摂取すると、それが胃や腸の中で物理的な壁のように働き、後から摂取される糖質の消化・吸収速度を遅らせます。これにより、血糖値の上昇が緩やかになるのです。日本の研究グループが医学雑誌『Journal of Clinical Biochemistry and Nutrition』で発表した研究でも、炭水化物の前に野菜を摂取することで、食後血糖値とインスリン分泌の両方が有意に抑制されることが明確に示されています (Imai, S. et al., 2014)。
- 生理的な「ブレーキ」効果: 近年の研究で特に注目されているのが、脂質の役割です。炭水化物を摂取する前に脂質を含む食品(例えば、オリーブオイルをかけたサラダやナッツ、魚など)を摂取すると、小腸からGLP-1(グルカゴン様ペプチド-1)という消化管ホルモンの分泌が促進されます。このGLP-1は、インスリンの分泌を促すだけでなく、胃の蠕動(ぜんどう)運動を緩やかにして食べたものが胃から小腸へ移動するスピードを遅らせる作用を持ちます。つまり、脂質が「消化のブレーキ」を踏むことで、糖質の吸収が時間的に分散され、血糖値の急上昇が抑制されるのです。オーストラリアの研究チームが医学雑誌『Diabetes Care』で報告した内容によると、脂質を糖質より30分前に摂取することで、食後血糖値の上昇が劇的に抑制されることが確認されています (Gentilcore, A. H. et al., 2006)。
これらを総合すると、食事の最初にサラダ、スープ、肉、魚といった副菜から箸をつけ、最後にご飯やパンなどの主食を食べるというシーケンスが、血糖コントロールの観点から極めて合理的であると言えるでしょう。
アプローチ2:食材の選択 — 「低GI/GL食」への戦略的シフト
次に重要なのが、摂取する炭水化物の「質」と「量」を意識することです。ここで指標となるのがGI(Glycemic Index)とGL(Glycemic Load)です。
- GI(グリセミック・インデックス): ある食品を摂取した後の血糖値の上昇度合いを、ブドウ糖を100とした場合の相対値で表したものです。高GI食品(白米、食パン、うどんなど)は血糖値を急激に上昇させやすく、低GI食品(玄米、全粒粉パン、オートミールなど)は上昇が緩やかです。
- GL(グリセミック・ロード): GIが「質」の指標であるのに対し、GLはそれに「量」の概念を加味した指標です。\( GL = (\text{各食品のGI値} \times \text{1食あたりの炭水化物量}[\text{g}]) \div 100 \) で計算され、より現実に即した血糖値への影響度を示します。
日常の食事において、高GI食品を低GI食品へ戦略的にシフトすることは、血糖コントロールの根幹をなします。例えば、ハーバード公衆衛生大学院などが参加した大規模な疫学研究では、白米の摂取量が多い集団と比較して、玄米を多く摂取する集団では2型糖尿病の発症リスクが有意に低いという関連が報告されています (Sun, Q. et al., 2010)。これは、玄米が持つ豊富な食物繊維やマグネシウムなどの栄養素が、複合的に血糖コントロールに寄与している可能性を示唆しています。
アプローチ3:「酢」の力を借りる — 食前・食中の「アシッド・ブレーキ」
古くからの生活の知恵である「食酢」の活用も、現代科学によってその有効性が検証されています。食前に大さじ1杯(約15ml)程度の酢を水などで希釈して飲む、あるいは食事中に酢の物やドレッシングなどで取り入れることで、食後の血糖値上昇を穏やかにする効果が期待できます。
このメカニズムの核心は、酢の主成分である酢酸(Acetic Acid)にあります。アリゾナ州立大学の研究チームが医学雑誌『Diabetes Care』で発表した論文によれば、酢酸にはいくつかの作用が考えられています (Johnston, C. S. & Gaas, C. A., 2006)。一つは、胃の排出速度を遅らせる効果(アプローチ1の脂質と類似の効果)、そしてもう一つは、炭水化物を分解する消化酵素(アミラーゼ)の働きを一部阻害する可能性です。これにより、糖の分解と吸収が遅延し、結果として血糖値の急上昇が抑制されると考えられています。
アプローチ4:食後の軽い運動 — 「15分ウォーキング」という即時投資
もし高GI/GLの食事を摂ってしまった場合でも、有効なリカバリープランが存在します。それは、食後15分から30分以内に軽い運動を開始することです。15分程度のウォーキングやその場での足踏みといった、心拍数が少し上がる程度の有酸素運動で十分な効果が期待できます。
運動が食後血糖に与える影響は劇的です。筋肉は、人体における最大のブドウ糖貯蔵庫であり、活動時には血液中のブドウ糖をエネルギー源として直接取り込みます。この糖の取り込みは、インスリンの働きとは独立したメカニズム(筋肉の収縮自体が、糖輸送担体であるGLUT4を細胞膜上へ移動させる)によっても促進されます。つまり、食後に筋肉を動かすことは、いわば「血糖値の緊急避難スイッチ」を入れるようなものなのです。
米国糖尿病学会(ADA)のポジション・ステートメントでも、食後の短時間のウォーキングなどが2型糖尿病患者の血糖コントロールを改善することが明記されており、その有効性は広く認知されています (Colberg, S. R. et al., 2016)。
アプローチ5:行動経済学の応用 — 「賢い選択」を自動化する仕組み
これら4つの科学的アプローチを知識として理解することと、それを日常生活で継続的に実践することの間には、大きな隔たりがあります。ここで、私の専門の一つである行動経済学の知見が極めて有効となります。
人間は、将来の大きな利益(長期的な健康)よりも、目先の小さな満足(美味しい高GI食品の誘惑)を優先してしまう「現在バイアス(Present Bias)」という認知的なクセを持っています。この不合理な性質を意志の力だけで克服しようとするのは、多くの場合、失敗に終わります。
重要なのは、意志力に頼るのではなく、賢い選択をせずにはいられない環境、すなわち「選択アーキテクチャ」を自らデザインすることです。これは、ノーベル経済学賞を受賞したリチャード・セイラーらが提唱する「ナッジ(Nudge)」の考え方に基づいています (Thaler, R. H., & Sunstein, C. R., 2008)。
具体的な戦略としては、以下のようなものが考えられます。
- デフォルト設定の変更:
- 食事の際は、必ず最初にサラダや具沢山のスープをテーブルに並べることを「デフォルト(初期設定)」にする。
- オフィスのデスクや自宅の目に見える場所には、間食としてナッツやハイカカオチョコレートなど、低GIの選択肢のみを置く。
- If-Thenプランニング(事前計画):
- 「もし昼食を食べ終えたら、オフィスの周りを10分歩く」「もし外食でパスタを注文するなら、必ずサラダをセットで頼む」といったように、「(状況)が起きたら、(行動)をする」というルールをあらかじめ具体的に決めておく。
これらの仕組みは、その都度の意思決定の認知的負荷を劇的に軽減し、無意識のうちに健康的な行動を促します。自らの行動パターンをシステムとして捉え、最適なアーキテクチャを設計することこそ、多忙な現代人が健康戦略を成功させるための鍵となるのです。
まとめ:血糖値のマネジメントは、未来の自分への最高の投資である
血糖値スパイクは、単なる食後の眠気や集中力の低下といった短期的なパフォーマンスの問題に留まりません。それは、日々の知的生産性を蝕み、長期的には私たちの健康資本を少しずつ損なっていく「静かなる脅威」であり、気づかぬうちに積み上がる「見えざる負債」とも言えます。
しかし、本稿で概観したように、私たちはこの課題に対して決して無力ではありません。そのメカニズムを正しく理解し、科学的根拠に基づいた戦略を日々の生活というシステムに実装することで、血糖カーブという重要な生体パラメータを、自らの手でコントロールすることが可能なのです。
血糖値のカーブを穏やかに保つこと。それは、日々のコンディションを安定させ、最高のパフォーマンスを発揮するための基盤を築く行為に他なりません。そしてそれは、未来の自分へ贈ることができる最高の投資です。なぜなら、その投資によって得られるリターンは、単なる健康寿命の延伸だけでなく、明晰な思考力、創造性、そして人生のあらゆる局面で最良の意思決定を下すための「認知資本」そのものだからです。この知的武装こそが、変化の激しい時代を生き抜くための、最も確かな礎となるでしょう。
参考文献
- Jenkins, D. J. A., Wolever, T. M. S., Taylor, R. H., Barker, H., Fielden, H., Baldwin, J. M., Bowling, A. C., Newman, H. C., Jenkins, A. L., & Goff, D. V. 1981. Glycemic index of foods: a physiological basis for carbohydrate exchange. The American Journal of Clinical Nutrition 34(3):362–366. doi:10.1093/ajcn/34.3.362 PMID:6259925
- Thaler, R. H., & Sunstein, C. R. 2008. Nudge: Improving decisions about health, wealth, and happiness. Yale University Press. 【NO-DOI】
- Brownlee, M. 2001. Biochemistry and molecular cell biology of diabetic complications. Nature 414(6865):813–820. doi:10.1038/414813a PMID:11742414
- American Diabetes Association. 2024. 6. Glycemic Goals and Hypoglycemia: Standards of Care in Diabetes—2024. Diabetes Care 47(Supplement_1):S111–S125. doi:10.2337/dc24-S006 PMID:38078580
- 日本糖尿病学会. 2019. 糖尿病診療ガイドライン2019【日本語】. 日本糖尿病学会. https://www.jds.or.jp/modules/publication/index.php?content_id=4 【NO-DOI】
- 厚生労働省. 2024. 健康日本21(第三次)【日本語】. 厚生労働省. https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/kenkou_iryou/kenkou/kenkounippon21/index.html 【NO-DOI】
- 厚生労働省. 2018. 医療広告ガイドライン【日本語】. 厚生労働省. https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/kenkou_iryou/iryou/kokokukisei/index.html 【NO-DOI】
- Zafar, M. I., Mills, K. E., Zheng, J., Peng, M., Ye, X., & Chen, L. L. 2023. Post-meal physical activity for postprandial glucose management in adults with type 2 diabetes: A systematic review and meta-analysis. Sports Medicine 53(9):1765–1780. doi:10.1007/s40279-023-01865-z PMID:37208639
- Koutoukidis, D. A., Astbury, N. M., De la Pera, A., Tudor, K., Morris, E., Henry, J. A., … & Jebb, S. A. 2023. The effect of meal-sequencing on glucose regulation, energy intake and other metabolic markers: a systematic review and meta-analysis. Clinical Nutrition 42(5):673–686. doi:10.1016/j.clnu.2023.03.007 PMID:36948017
- Buffey, A. J., Herring, M. P., Langley, C., Donnelly, A. E., & Carson, B. P. 2022. The Acute Effects of Interrupting Prolonged Sitting Time in Adults: A Systematic Review and Meta-analysis. Sports Medicine 52(10):2411–2430. doi:10.1007/s40279-022-01649-9 PMID:35133642
- Shishehbor, F., Shirani, F., & Salehi-Abargouei, A. 2021. Effect of vinegar consumption on cardiometabolic risk factors: a systematic review and meta-analysis of randomized controlled trials. European Journal of Nutrition 60(6):2969–2986. doi:10.1007/s00394-020-02462-y PMID:33420445
- Augustin, L. S. A., Kendall, C. W. C., Jenkins, D. J. A., Willett, W. C., Astrup, A., Barclay, A. W., … & Poli, A. 2019. Glycemic index, glycemic load and glycemic response: an International Scientific Consensus Summit from the International Carbohydrate Quality Consortium (ICQC). Nutrition, Metabolism and Cardiovascular Diseases 29(5):547–551. doi:10.1016/j.numecd.2019.02.006 PMID:30987895
- Nishimura, M., Fujita, S., Tsuchiya, Y., Hamaoka, T., & Tanaka, R. 2019. A practical approach to modifying postprandial hyperglycemia by altering the dinner menu. Journal of Nutritional Science and Vitaminology 65(3):233–239. doi:10.3177/jnsv.65.233 PMID:31257218
- Shukla, A. P., Iliescu, R. G., Thomas, C. E., & Aronne, L. J. 2015. Food Order Has a Significant Impact on Postprandial Glucose and Insulin Levels. Diabetes Care 38(7):e98–e99. doi:10.2337/dc15-0429 PMID:26106234
- Imai, S., Fukui, M., Kajiyama, S., Mizutani, S., Park, H., Asano, M., … & Nakano, T. 2014. Effect of eating vegetables before carbohydrates on glucose excursions in patients with type 2 diabetes. Journal of Clinical Biochemistry and Nutrition 54(1):7–11. doi:10.3164/jcbn.13-67 PMID:24426723
- Sun, Q., Spiegelman, D., van Dam, R. M., Holmes, M. D., Malik, V. S., Willett, W. C., & Hu, F. B. 2010. White rice, brown rice, and risk of type 2 diabetes in US men and women. Archives of Internal Medicine 170(11):961–969. doi:10.1001/archinternmed.2010.109 PMID:20516402
- Gentilcore, A. H., Chaikomin, R., Jones, K. L., Russo, A., Feinle-Bisset, C., Wishart, J. M., Rayner, C. K., & Horowitz, M. 2006. Effects of fat on gastric emptying of and the glycemic, insulin, and incretin responses to a carbohydrate meal in type 2 diabetes. Diabetes Care 29(10):2232–2237. doi:10.2337/dc06-1099 PMID:17003299
- D’Cunha, N. M., Naumovski, N., McKune, A. J., Isbel, S., & Kellett, J. 2022. A Narrative Review of the Evidence for Classifying Food Proteins as Either “Fast” or “Slow”‐Absorbed. Foods 11(3):342. doi:10.3390/foods11030342 PMID:35159491
- Holst, J. J., & Rosenkilde, M. M. 2018. GIP as a therapeutic target in diabetes and obesity: insight from incretin co-agonists. Journal of the Endocrine Society 2(9):1095–1108. doi:10.1210/js.2018-00187 PMID:30206775
- Colberg, S. R., Sigal, R. J., Yardley, J. E., Riddell, M. C., Dunstan, D. W., Dempsey, P. C., … & Tate, D. F. 2016. Physical Activity/Exercise and Diabetes: A Position Statement of the American Diabetes Association. Diabetes Care 39(11):2065–2079. doi:10.2337/dc16-1728 PMID:27926890
- Drucker, D. J., & Nauck, M. A. 2010. The incretin system: glucagon-like peptide-1 receptor agonists and dipeptidyl peptidase-4 inhibitors in type 2 diabetes. The Lancet 368(9548):1696–1705. doi:10.1016/S0140-6736(06)69705-5 PMID:17098089
- Johnston, C. S., & Gaas, C. A. 2006. Vinegar: medicinal uses and antiglycemic effect. Medscape General Medicine 8(2):61. PMID:16926800
- Ceriello, A. 2005. Postprandial hyperglycemia and diabetes complications: is it time to treat? Diabetes 54(1):1–7. doi:10.2337/diabetes.54.1.1 PMID:15616015
- Service, F. J. 1983. Hypoglycemic disorders. New England Journal of Medicine 308(16):949-957. 【NO-DOI】 PMID:6340428
- Kahneman, D. 2020. Thinking, Fast and Slow. Farrar, Straus and Giroux. 【NO-DOI】
- Gollwitzer, P. M., & Oettingen, G. 2016. Planning promotes goal striving. In K. D. Vohs & R. F. Baumeister (Eds.), Handbook of self-regulation: Research, theory, and applications (pp. 223-244). The Guilford Press. 【NO-DOI】
ご利用規約(免責事項)
当サイト(以下「本サイト」といいます)をご利用になる前に、本ご利用規約(以下「本規約」といいます)をよくお読みください。本サイトを利用された時点で、利用者は本規約の全ての条項に同意したものとみなします。
第1条(目的と情報の性質)
- 本サイトは、医療分野におけるAI技術に関する一般的な情報提供および技術的な学習機会の提供を唯一の目的とします。
- 本サイトで提供されるすべてのコンテンツ(文章、図表、コード、データセットの紹介等を含みますが、これらに限定されません)は、一般的な学習参考用であり、いかなる場合も医学的な助言、診断、治療、またはこれらに準ずる行為(以下「医行為等」といいます)を提供するものではありません。
- 本サイトのコンテンツは、特定の製品、技術、または治療法の有効性、安全性を保証、推奨、または広告・販売促進するものではありません。紹介する技術には研究開発段階のものが含まれており、その臨床応用には、さらなる研究と国内外の規制当局による正式な承認が別途必要です。
- 本サイトは、情報提供を目的としたものであり、特定の治療法を推奨するものではありません。健康に関するご懸念やご相談は、必ず専門の医療機関にご相談ください。
第2条(法令等の遵守)
利用者は、本サイトの利用にあたり、医師法、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(薬機法)、個人情報の保護に関する法律、医療法、医療広告ガイドライン、その他関連する国内外の全ての法令、条例、規則、および各省庁・学会等が定める最新のガイドライン等を、自らの責任において遵守するものとします。これらの適用判断についても、利用者が自ら関係各所に確認するものとし、本サイトは一切の責任を負いません。
第3条(医療行為における責任)
- 本サイトで紹介するAI技術・手法は、あくまで研究段階の技術的解説であり、実際の臨床現場での診断・治療を代替、補助、または推奨するものでは一切ありません。
- 医行為等に関する最終的な判断、決定、およびそれに伴う一切の責任は、必ず法律上その資格を認められた医療専門家(医師、歯科医師等)が負うものとします。AIによる出力を、資格を有する専門家による独立した検証および判断を経ずに利用することを固く禁じます。
- 本サイトの情報に基づくいかなる行為によって利用者または第三者に損害が生じた場合も、本サイト運営者は一切の責任を負いません。実際の臨床判断に際しては、必ず担当の医療専門家にご相談ください。本サイトの利用によって、利用者と本サイト運営者の間に、医師と患者の関係、またはその他いかなる専門的な関係も成立するものではありません。
第4条(情報の正確性・完全性・有用性)
- 本サイトは、掲載する情報(数値、事例、ソースコード、ライブラリのバージョン等)の正確性、完全性、網羅性、有用性、特定目的への適合性、その他一切の事項について、何ら保証するものではありません。
- 掲載情報は執筆時点のものであり、予告なく変更または削除されることがあります。また、技術の進展、ライブラリの更新等により、情報は古くなる可能性があります。利用者は、必ず自身で公式ドキュメント等の最新情報を確認し、自らの責任で情報を利用するものとします。
第5条(AI生成コンテンツに関する注意事項)
本サイトのコンテンツには、AIによる提案を基に作成された部分が含まれる場合がありますが、公開にあたっては人間による監修・編集を経ています。利用者が生成AI等を用いる際は、ハルシネーション(事実に基づかない情報の生成)やバイアスのリスクが内在することを十分に理解し、その出力を鵜呑みにすることなく、必ず専門家による検証を行うものとします。
第6条(知的財産権)
- 本サイトを構成するすべてのコンテンツに関する著作権、商標権、その他一切の知的財産権は、本サイト運営者または正当な権利を有する第三者に帰属します。
- 本サイトのコンテンツを引用、転載、複製、改変、その他の二次利用を行う場合は、著作権法その他関連法規を遵守し、必ず出典を明記するとともに、権利者の許諾を得るなど、適切な手続きを自らの責任で行うものとします。
第7条(プライバシー・倫理)
本サイトで紹介または言及されるデータセット等を利用する場合、利用者は当該データセットに付随するライセンス条件および研究倫理指針を厳格に遵守し、個人情報の匿名化や同意取得の確認など、適用される法規制に基づき必要とされるすべての措置を、自らの責任において講じるものとします。
第8条(利用環境)
本サイトで紹介するソースコードやライブラリは、執筆時点で特定のバージョンおよび実行環境(OS、ハードウェア、依存パッケージ等)を前提としています。利用者の環境における動作を保証するものではなく、互換性の問題等に起因するいかなる不利益・損害についても、本サイト運営者は責任を負いません。
第9条(免責事項)
- 本サイト運営者は、利用者が本サイトを利用したこと、または利用できなかったことによって生じる一切の損害(直接損害、間接損害、付随的損害、特別損害、懲罰的損害、逸失利益、データの消失、プログラムの毀損等を含みますが、これらに限定されません)について、その原因の如何を問わず、一切の法的責任を負わないものとします。
- 本サイトの利用は、学習および研究目的に限定されるものとし、それ以外の目的での利用はご遠慮ください。
- 本サイトの利用に関連して、利用者と第三者との間で紛争が生じた場合、利用者は自らの費用と責任においてこれを解決するものとし、本サイト運営者に一切の迷惑または損害を与えないものとします。
- 本サイト運営者は、いつでも予告なく本サイトの運営を中断、中止、または内容を変更できるものとし、これによって利用者に生じたいかなる損害についても責任を負いません。
第10条(規約の変更)
本サイト運営者は、必要と判断した場合、利用者の承諾を得ることなく、いつでも本規約を変更することができます。変更後の規約は、本サイト上に掲載された時点で効力を生じるものとし、利用者は変更後の規約に拘束されるものとします。
第11条(準拠法および合意管轄)
本規約の解釈にあたっては、日本法を準拠法とします。本サイトの利用および本規約に関連して生じる一切の紛争については、東京地方裁判所を第一審の専属的合意管轄裁判所とします。